

 �����Ź��ں�
�����Ź��ں�
 ������è�콢��
������è�콢��


 �����Ź��ں�
�����Ź��ں�
 ������è�콢��
������è�콢��




������Χ
�����涨��ʳƷ�г��˾��ƣ�Enterobacteriaceae���ļ��鷽����
������һ�������ڳ��˾��ƺ����ϸߵ�ʳƷ�г��˾��Ƶļ������ڶ��������ڳ��˾��ƺ����ϵ�ʳƷ�г��˾��Ƶļ�����
�� ����Ͷ���
��.��
���˾��ơ�
�ڸ��������·��������Dz��ᡢ����ø���Ե��������������������������ѿ���˾���
��.��
���˾��Ƽ�����
�������涨��������ÿ�˻�ÿ���������еij��˾��ƽ��м�����
��.��
���������
���ڲ��ɷֲ���һ�ּ�Ӽ���������
�� �豸�Ͳ���
������ʵ���ҳ�������������豸�⣬�����豸�Ͳ������£�
�����������������䣺���� ����� �档
�����������䣺�� �桫�� �档
��������ˮԡ�䣺���� ����� �档
����������ƽ�������������硣
��������������������������������
����������������
��������������
�������������ܣ������̣��ߣ����������� �̶ȣ����������̣��ߣ��������� �̶ȣ�������Һ������ͷ��
������������ƿ���Ч�������������������̡����������̡�
������������������ֱ������������
�������������Թܣ���������������������������������������������
������������� �ƻ��� ��ɫ�ܻ��ܣ�� ��ֽ��
�������������Լ�
�����������嵰����ˮ���£Уף������£�����
�����������������ǻ��̵����������ţ� �����������£�����
���������ᾧ�����Ժ쵨����������֬���֣ң£ǣ��������£�����
��������Ӫ����֬���Σ��������£�����
����������������֬�����£�����
��������������ȾɫҺ�����£�����
������������ø�Լ������£�����
����������������죯�̣Σ�ϣȣ����£�����
����������������죯�� �ȣã죺���£�����
��һ�������˾���ƽ�������
�����������
���˾���ƽ���������������ͼ����
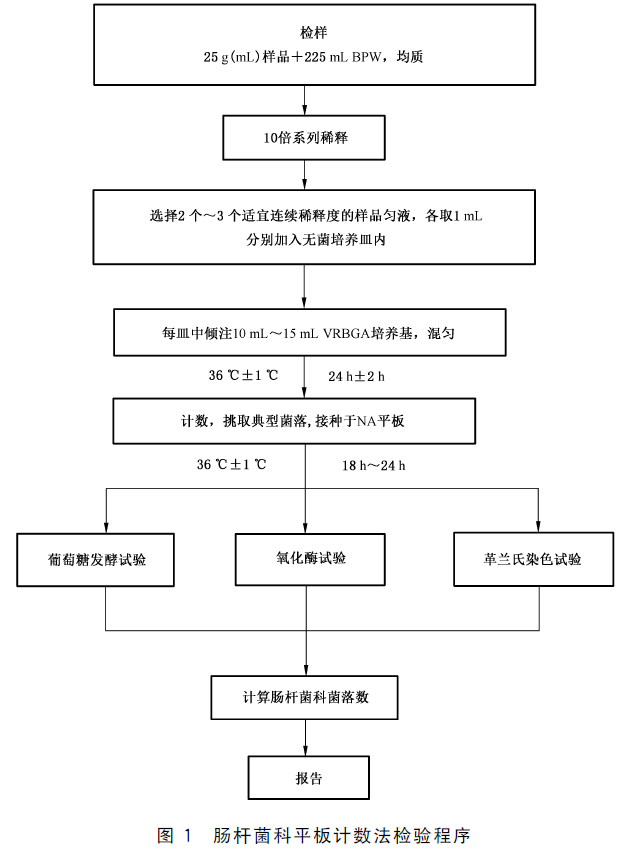
������������
����������Ʒ��ϡ��
����������������Ͱ������Ʒ����ȡ������ ��Ʒ����ʢ�У����� ���̣£У� �������ʱ��У������������������������������ʣ� ���������������ʢ�У����� ���� �£У� �������ʴ��У����Ļ�ʽ�������Ĵ��������������Ƴɣ��ã�������Ʒ��Һ��
������������Һ����Ʒ������������ȡ�������� ��Ʒ����ʢ�У��������̣£У� ������ƿ��ƿ��Ԥ���ʵ��������������飩�У���ֻ��ȣ��Ƴɣ��ã�������Ʒ��Һ��
�������������ã����� �����ܻ�����Һ����ȡ���ã�����Ʒ��Һ�����̣��عܱڻ���ע��ʢ�У����̣£У� �����Թ��У�ע�����ܻ���ͷ��˲�Ӧ����ϡ��Һ�棩����ҡ�Թܻ��ã�֧�� ���� �����ܷ�������ʹ���Ͼ��ȣ��Ƴɣ��ã���������Ʒ��Һ��
�������������������������������������Ƴɣ���������ϵ��ϡ����Ʒ��Һ��ÿ����ϡ�ͣ��Σ����ã�֧������ �������ܻ���ͷ�����Ʊ���Ʒ��Һ����Ʒ������ϣ�ȫ���̲��ó�����������
����������עƽ�������
���������������ݶ���Ʒ��Ⱦ״���Ĺ��Ƽ��������Ҫ��ѡ�����������˵�����ϡ�Ͷȵ���Ʒ��Һ��Һ����Ʒ����ѡ��ԭҺ����ÿ��ϡ�ͶȽ��֣�����ƽ��ͬʱ���ֱ���ȡ�����̣£У� ����������ƽ������Ϊ�հ��ա�
���������������������̡��������� ��ȴ������ ��ģ֣ң£ǣ����ɷ����ڣ��� ����� �����ˮԡ���б��£���ע��ÿ��ƽ���С�С����תƽ��ʹ��Ʒ��Һ����������ֻ��ȡ�
����������������֬���̺���עһ����ͬ��������������ƽ����㡣��ֹ����������ʹ����������Ϊ
���ԡ�
���������������֣ң£ǣ� ƽ���ϲ���֬���̺�תƽ�壬���� ����� �����������衫�����衣
�����������;��������ȷ��
���������������˾��Ƶ��;���Ϊ�л��������ķۺ�ɫ����ɫ����ɫ���䡣ѡȡ���;������ڣ����ãƣա��������ãƣ� ֮�䡢�����Ӿ���������ƽ�壬ֻ�������;���������������Ծ����γɵ�λ���ãƣգ���ʾ��
����������������һ��ƽ���нϴ�Ƭ״��������ʱ�����˲��ã���Ӧ����Ƭ״����������ƽ����Ϊ��ϡ��
�ȵľ���������Ƭ״���䲻��ƽ���һ�룬������һ���о���ֲ��ֺܾ��ȣ����ɼ�����ƽ��������������һ��ƽ���������
��������������ƽ���ϳ��־���������Խ��ߵ���״����ʱ����ÿ��������Ϊһ�����������
��������������ÿ��ƽ����������ȡ������С�ڣ���ȫѡ�����;������ȷ�ϣ�����в�ͬ��̬�ĵ��;��䣬��ÿ����̬�ֱ�������ȡ�����������ȷ�ϡ�
���������������;����ȷ�ϣ�
�ᣩ���ֱ�����ѡ��ÿһ�����䣬������Ӫ����֬ƽ�壬���� ����� �����������衫�����裬��ȡƽ�����ľ�����и�����Ⱦɫ���졢����ø���鼰�����Ƿ������顣
�⣩��������Ⱦɫ���죺���˾���Ϊ���������Ը˾�����ѿ�ߣ���СΪ�������������������̣��� �������������������̣���
�㣩������ø���飺�ò���ҿ���ֻ�����������Ҫ���������ֻ�����ȡ��������Ϳ�ڽ�ʪ����ø�Լ�����ֽ�ϣ���ֽ����ɫ�ڣ������ڱ������ɫ����Ϊ���Է�Ӧ��
�䣩�������Ƿ������飺�ý�������ȡ��������ø���Ե�ͬһ�����䣬��������������֬�ڣ��ڣ��� ���
�� ����������������裬���Թ��ڵ��������Ϊ��ɫ����Ϊ���Է�Ӧ��
������������ļ���
������������һ��ԭ��
������������ϡ�Ͷȵ�ƽ����;����������˼�����Χ�ڣ���ʽ���������㣬ʾ������������������������������������
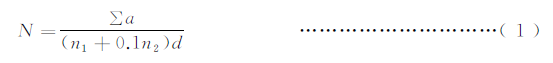
��ʽ�У�
N��������Ʒ�г��˾��ƾ�������
��a������ȷ֤�ij��˾��ƾ�����֮�ͣ�
n1 ��������һϡ�Ͷȣ���ϡ�ͱ�����ƽ���������ȷ֤�ij��˾��ƾ��䣩��
n2 �������ڶ�ϡ�Ͷȣ���ϡ�ͱ�����ƽ���������ȷ֤�ij��˾��ƾ��䣩��
d������ϡ�����ӣ���һϡ�Ͷȣ���
���У�a��ʽ���������㣺
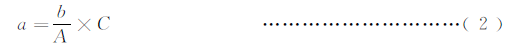
��ʽ�У�
a������ȷ֤�ij��˾��ƾ�������
b������ijһƽ���Р��������б�ȷ֤Ϊ���˾��Ƶľ�������b��A��
A������ijһƽ��������ȷ������ľ�������
C������ijһƽ���е��;���������
�������������;�����
�����ϡ�Ͷȣ�����Һ����ƷԭҺ��ƽ��ĵ��;�������С�ڣ����ãƣգ�����ȷ֤�ij��˾��ƾ��䣬
����ȷ֤�ľ������������ϡ�ͱ������㡣
�����ϡ�Ͷȣ�����Һ����ƷԭҺ��ƽ�����������������;�������С�ڣ����ãƣգ�����ȷ֤��
���˾��ƾ��䣬����С�ڣ��������ϡ�ͱ������㡣
�������������������
��һϡ�Ͷ�ƽ���ϵĵ��;����������ڣ������ãƣգ�����ȷ֤�ij��˾��ƾ��䣬�Լ��ڶ�ϡ�Ͷ�ƽ������ȷ֤�ij��˾��ƾ������;��������ڣ����ãƣա��������ãƣ� ֮�䣬����ȷ֤�ľ��������Ե�һϡ�ͱ������㣬ʾ������������
������ϡ�Ͷȵ�ƽ���ϵ��;��������������˼�����Χ�ڣ�����ȷ֤�ij��˾��ƾ��䣬����С�ڣ��������ϡ�ͱ������㡣
��������
��������������С�ڣ�����ʱ�����������档
�����������������ڻ���ڣ�����ʱ���Եڣ�λ���ֽ�����Լ��ȡǰ��λ���֣������ã�����λ����Ҳ����������ָ����ʽ����ʾ��������λ��Ч���֡�
��������������Լ�����������롱ԭ����С�
��������������ƽ����Ϊ���Ӿ��������������������ӡ�
�����������հ������о�����������˴μ������Ч��
������������ȡ���ԣãƣգ���Ϊ��λ���棬���ȡ���ԣãƣգ����� Ϊ��λ���档
�ڶ��������˾��Ơ͠Рμ�����
�����������
���˾��ƣͣУ� ��������������ͼ����
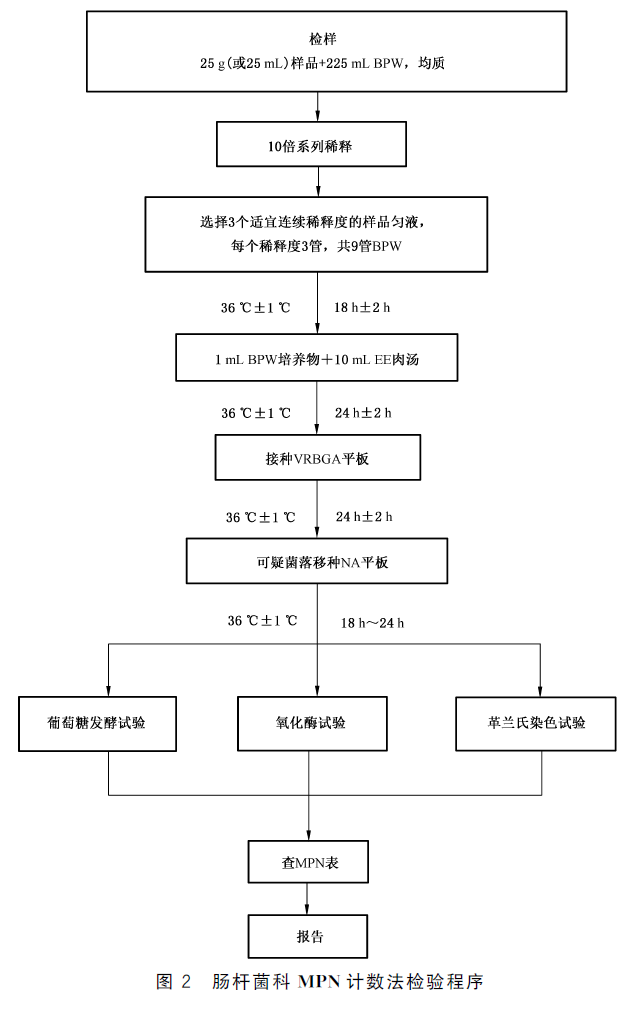
������������
����������Ʒ��ϡ��
������������
�����������ֺ�����
��������������ѡ����ǰ����
���ݶ���Ʒ��Ⱦ״���Ĺ��Ƽ��������Ҫ��ѡ�� ����������ϡ�Ͷȵ���Ʒ��Һ��ÿ��ϡ�Ͷ����ܣ������ܣ£У� �ڣ��� �� ���� ����������������衣
������������ѡ��������
�ӣ£У� ���������У��ֱ���ȡ������ ����������ڣ������� �ģţ� �����У��������������������������衣
����������������
�ý��ֻ��ӣţ� ���������зֱ�ȡ������������߽����ڣ֣ң£ǣ� ƽ�壬���� ����� ����������������裬�۲�ƽ���������;��䡣
�����������;����ȷ��
���;���ȷ�ϼ���������
����������
���˾���Ϊ������������ѿ���˾������������Dz��ᡢ����ø���ԡ�ֻҪ�У�������ȷ��Ϊ���˾��ƣ����������ģţ� �ܼ�Ϊ���˾������ԣ����ݣţ� ���Թ�����ͣУ� ��������¼�ã�������ÿ�ˣ���������Ʒ�г��˾��ƵģͣУ� ֵ������ȡ���ԣͣУΣ���Ϊ��λ���棬���ȡ���ԣͣУΣ����� Ϊ��λ���档
ʵ�������Ʒһ�����������Ʒ���Ƽ��ɽ����Ʒ����ҳ������
| ��Ʒ���� | ��Ʒ���� | ���g�� | �۸�(Ԫ) | ��Ʒ˵������; |
| HB0109 | Ӫ����֬��NA�� | 250g | 90 | ϸ�������������ǣ�����Ѫ��֬�����ʹ�����(GB��) |
| HB4084 | ���嵰����ˮ��BPW�� | 250g | 70 | ��������˾�ǰ����������GB���� |
| HB0126-7 | ���������ǻ��̵���������EE������ | 250g | 250 | ÿ֧������200ml |
| HB0176-4 | �ᾧ�����Ժ쵨��������������VRBGA�� | 250g | 105 | ���ڷ���С���᳦��Ү��ɭ�Ͼ� |
| HB0135-2 | ��������֬ | 250g | 120 | ����С���᳦��Ү��ɭ�Ͼ��������� |
| HB8278 | ������ȾɫҺ | 5ml*8 | 40 | ����������������С���᳦��Ү��ɭ�Ͼ���������Ӧɸѡ |
| JX3400094 | ����ø�Լ� | 1g | 50 | ����������������С���᳦��Ү��ɭ�Ͼ���������Ӧɸѡ |
��һƪ��GBT 4789.8-2016С���᳦��Ү��ɭ�Ͼ�����
��һƪ��ʲô��Ʒ���Ը������



